aggregatszustände
Mit dem Kugelteilchenmodell und der Eigenbewegung der kleinsten Teilchen lassen sich nicht nur die Diffusion, sondern auch die Aggregatzustände und die Übergänge zwischen ihnen anschaulich erklären.
|
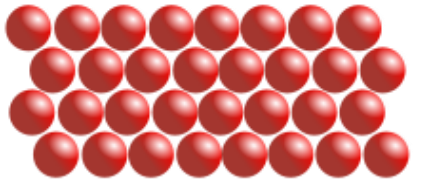
Reinstoffe in festem Zustand
Zwischen den kleinsten Teilchen wirken starke Anziehungskräfte, welche die Kugelteilchen auf ihren Plätzen festhalten. Um diese können die Teilchen schwingen. Je grösser die Anziehungskräfte zwischen den Teilchen sind, umso höher ist die Schmelztemperatur des Stoffes und umso grösser ist seine Härte. Die kleinsten Teilchen sind dicht nebeneinander angeordnet, deshalb lässt sich ein Feststoff kaum zusammenpressen. Auch die Kristallform vieler Feststoffe ist auf die regelmässige Anordnung der kleinsten Teilchen zurückzuführen. |
|
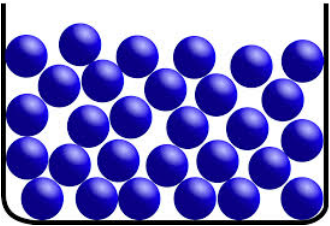
Reinstoffe in flüssigem Zustand
Auch Flüssigkeiten lassen sich kaum zusammendrücken, aber sie sind beweglich, lassen sich verformen und passen sich jeder Gefässform an. Offensichtlich sind die Anziehungskräfte zwischen den Teilchen geringer als bei Feststoffen. Deshalb sind die kleinsten Teilchen einer Flüssigkeit leicht gegeneinander beweglich. Dass die Anziehungskräfte dennoch vorhanden sind, zeigt der Zusammenhalt eines Wassertropfens. Die Abstände zwischen den Teilchen sind gering, aber meist grösser als im Feststoff. |
|
Reinstoffe in gasförmigen Zustand
Ein Gas lässt sich im Gegensatz zu einer Flüssigkeit oder einem Feststoff leicht zusammendrücken, es nimmt auch jeden zur Verfügung stehenden Raum ein. Dies lässt sich damit erklären, dass sich die kleinsten Teilchen eines Gases sehr weit voneinander entfernen können, weil nur sehr geringe Anziehungskräfte zwischen ihnen wirken. Die Teilchen bewegen sich frei und ungeordnet im Raum. |
übergänge zwischen den aggregatszuständen
|
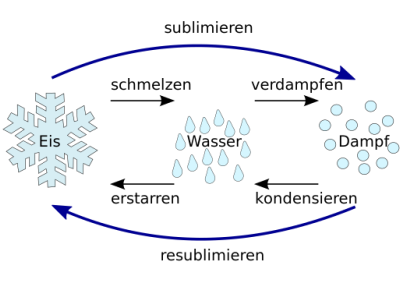
Übergänge zwischen den Aggregatzuständen
Erwärmt man einen Feststoff, so dehnt er sich aus. Die Wärmezufuhr führt zu heftigeren Schwingungen der kleinsten Teilchen, der Abstand zwischen den kleinsten Teilchen nimmt zu, die Anziehungskräfte zwischen ihnen werden dadurch kleiner. Schliesslich werden die Schwingungen so gross, dass die Teilchen ihre Plätze verlassen, die regelmässige Anordnung der Teilchen geht verloren, die Teilchen verschieben sich gegeneinander. Der Stoff schmilzt. Bei weiterer Wärmezufuhr bewegen sich die kleinsten Teilchen immer schneller, ihre Abstände zueinander vergrössern sich weiter, bis schliesslich die Anziehungskräfte zwischen ihnen überwunden werden. Der Stoff verdampft (siedet). Während des Schmelz- und Siedevorgangs ändert sich die Temperatur eines Reinstoffes auch bei weiterer Wärmezufuhr nicht. Die zugeführte Wärme dient dazu, die Teilchenabstände zu vergrössern und die Anziehungskräfte zu überwinden. Es tritt so lange keine Temperaturerhöhung ein, bis der gesamte Stoff in den flüssigen oder gasförmigen Aggregatzustand übergegangen ist. Das Verdunsten einer Flüssigkeit lässt den Schluss zu, dass auch unterhalb der Siedetemperatur einzelne Teilchen die Flüssigkeit verlassen können. Auch die Oberfläche eines Feststoffes können einzelne Teilchen verlassen, wenn die Anziehungskräfte nicht sehr hoch sind. Der Stoff sublimiert. |